发布时间:2018-06-06 09:24 类别:医学话题 标签: 来源:上海细胞治疗集团绍兴分中心 作者:医学资源分享
公元前2625年,古埃及医生印和阗将失望的病人送出门外。在他的病历上,风轻轻吹过,乳腺癌的诊断落进印和阗的眼里,在治疗一栏中,“没有疗法”四个字如此刺眼。
这是人类有史记载的第一例乳腺癌患者。
人类同癌症长达4000多年的战争中,无数药物和疗法如过江之鲤鱼不计其数,各种偏方层出不穷。印和阗如果来到2018年,看到如今乳腺癌的5年生存率可以超过90%,相信一定会十分欣慰,治疗那一栏中,也不再将是没有疗法。
1809年,人类历史上第一个手术病例诞生,如今手术治疗已经成为早期癌症和未转移癌症的最有效治疗手段;而在其后的1895年,我们用X线和镭来治疗癌症,拉开了放疗的序幕;20世纪40年代,曾经在二战时期令人惊惧万分的生化武器芥子气弃暗投明,打开了人类化疗的大门。


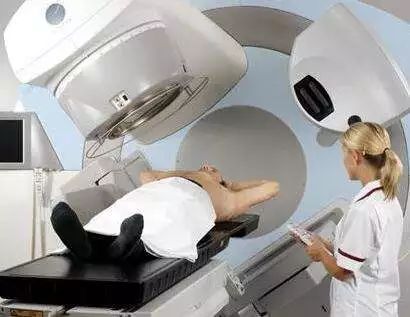
手术使得人类早期癌症的治愈率攀升到了一个新的台阶,放化疗如今随着药物和剂量的改进以及配套的辅佐药物的生产,副作用正在不断降低。但是这些治疗手段虽然帮助人类在抗癌战争中赢得了局部战役的胜利,但是想要最终取得战争的胜利,我们还需要新的武器。
于是,一个崭新的抗癌疗法——免疫疗法登上了历史舞台。
沉浮百年——免疫疗法的前世今生
公元846年,来自塞纳河畔的诺曼人气势汹汹的进攻法国巴黎,久经血与火考验的战士丝毫不畏惧着洒热血,然而等待他们的,却是一场惨烈的“屠杀”。
当一个士兵脸上长了痘痘的时候,还被年长的士兵嘲笑,然而第二天,他们就笑不起来了——大批大批的士兵开始高烧,长痘,痘痘里面开始流出脓水,然后开始有士兵死去,接连不断。满怀着豪气的诺曼人首领惊恐的看着“瘟疫”蔓延,死去的人日起增多,哀嚎遍野,于是诺曼人首领下令:杀掉所有患病的士兵和看护的医生和护士。
这是当时唯一的办法。这个恐怖的疾病肆掠整个地球,在18世纪的时候,因为这个疾病,1亿5000万人因此死去。这个恐怖的疾病,就是天花。
然而,可能现在我们对于天花都略显陌生,甚至鲜有听见这个名词,因为对于天花,我们有了特效药。
1796年5月17日,英国内科医生琴纳给自己送上了一份特别的礼物,也为人类送上了一份堪称奇迹的礼物。在琴纳的诊室里,菲普士嘴里正吃着一根棒棒糖,他并不知道在百年之后他会因为成为第一个接种天花疫苗的人而被铭刻进历史,他此时只是在想着接下来是不是该和艾伦一起去草地玩耍。
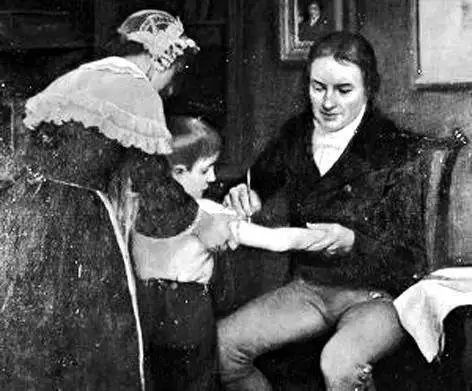
琴纳在为儿童注射牛痘
当挤牛奶的姑娘尼姆斯进来的时候,菲普士好奇的盯着尼姆斯的手,因为她的手上长着小小的天花脓疱。琴纳小心的在菲普士的手臂上划了一道痕迹,将尼姆斯的脓疱里面的脓浆滴到菲普士手臂上的划痕处。几周后,琴纳再次给菲普士接种了完整的天花病毒,然而,菲普士并没有感染天花!
这个肆掠了欧洲大陆几个世纪、堪称最恶劣的传染病、夺走了数亿生命的天花,就这样被人类攻克了。而与此同时,倒下的天花为人类树立了一个崭新的学科:现代免疫学。我们开始认识到人体并不想我们想象的那么脆弱,因为我们有着强大的免疫系统。
即使是强大的天花,同样被小小的疫苗攻克,这其中人体的免疫系统居功至伟。那么,在癌症治疗中,我们的免疫系统可不可以同样发挥神奇的作用呢?
19世纪80年代初,一名反复发作的恶性肉瘤患者的案例引起了William Coley的兴趣。这位患者在手术过程中不幸意外感染了化脓性链球菌,在没有抗生素的情况下,患者只能依靠自身的免疫力对抗病菌,也可以说:听天由命。然而命运终究是站在人类这一边:患者在经历几次高烧后,不仅链球菌的感染出现缓解,连其反复发作的恶性肉瘤也神奇的消失了!
William Coley开始意识到:人类的免疫系统远比我们想象的强大,于是Coley开始利用链球菌感染治疗恶性肉瘤来进行治疗。医学的历史往往都是由特殊的病例揭开,这个神奇自愈的病人不仅救活了自己,同时成就了William Coley“肿瘤免疫治疗之父”之名,而Coley也正式开启了人类肿瘤免疫治疗的篇章。

William Coley
20世纪初,德国药物学家Paul Ehrlich提出了侧链形成学说,为人类勾勒出了抗原抗体的雏形——我们如今的免疫治疗治疗理念都源于此。1908年,他与创立了细胞吞噬学说的俄国科学家Elie Metchnikoff登上了科学界最顶尖的领奖台——诺贝尔奖的领奖台,一起摘得了诺贝尔生理与医学奖。而由此,人类关于免疫学科的理论框架终于成功建立。

Paul Ehrlich
1957年,Thomas和Burnet提出了“免疫监视”学说,认为免疫系统具有区分并抑制肿瘤细胞生长的能力。然而在1974年,Osias Stutman“证明”裸鼠免疫系统与肿瘤发生无关,这个“证明”使得肿瘤的免疫疗法陷入了真正的低谷:如果免疫系统和肿瘤发生无关,那么这个疗法将被完全搁置。来自理论的危机使得坚信免疫疗法的前路蒙上了一层厚厚的阴霾。
但是,每逢穷困之际,则必有奇才横空而来。1984 年,Rosenberg 在临床试验中利用IL-2治愈了黑色素瘤患者,表明免疫系统确实可以遏制肿瘤发展,而在其后,Rosenberg又开创了LAK细胞疗法和TILs细胞疗法,证明:免疫系统在癌症治疗中占据着不可撼动的作用。
当理论和实践出现截然相反的时候,人们便不得不正视实践成果,重新审视理论。于是在2002年,Schreiber发表了免疫编辑理论,将癌症的发生发展分为免疫清除、免疫均衡和免疫逃逸3个阶段,从而为癌症的免疫治疗提供了坚实的理论基础,由此,拉开了肿瘤癌症免疫治疗的辉煌时代——PD-1、CAR-T和癌症疫苗开始真正走到攻克癌症的前沿位置。
乱花渐欲迷人眼——形形色色的癌症免疫疗法
癌症免疫疗法,顾名思义,是通过增强自身免疫功能来清除肿瘤细胞的技术。从21世纪以来,免疫疗法开始逐渐的变得成熟起来,由此衍生出了不同的分支,广义上可分为四个主要类别:非特异性免疫增强剂、疫苗、过继疗法和免疫检查点抑制剂。
1. 非特异性免疫增强剂:杀敌一千,自损八百

非特异性免疫增强剂主要通过整体上调机体的免疫功能来治疗癌症。最常见的非特异性免疫增强剂包括白介素Interleukins和干扰素Interferons等。虽然增强剂使机体的免疫能力上升,但它并没有提高我们体内免疫细胞识别敌我细胞的能力,大幅提升免疫细胞攻击癌细胞的能力的代价是大量的“误伤”人体的正常细胞,带来严重的副作用如,流感样症状、皮疹、白细胞减少等。由于非特异性免疫增强剂“杀敌一千,自损八百”的效果,通常与其他免疫疗法或化疗联合使用进行治疗。
2. 癌症疫苗:预防治疗两手抓
自从1796年牛痘疫苗被用以预防天花,疫苗就成为人类与疾病斗争的有力武器之一。目前经美国FDA批准用于癌症治疗的疫苗共有四种,分别是用于预防宫颈癌的Gardasil与 Cervarix、用于预防肝癌的乙肝疫苗和用于治疗晚期前列腺癌的Provenge。
九价HPV疫苗、乙肝疫苗
“曲线救国”预防癌症
人乳头瘤病毒HPV被认为是90%以上的宫颈癌的诱因,其中高致病性的16、18、31、33、45、52、58七类亚型都可通过接种九价HPV疫苗进行预防。同样地,在中国90%以上的原发性肝癌患者均为HBsAg阳性的乙肝患者,通过接种乙肝疫苗可大大降低罹患肝癌的概率。
Provenge
治疗性疫苗
与通过预防癌症相关病毒感染而“曲线救国”的预防性癌症疫苗不同,由Dendreon公司开发的治疗性癌症疫苗Provenge可以称的上是第一款真正意义上的癌症疫苗。Dendreon公司将患者体内的树突状细胞分离出,在体外对其进行改造成能识别前列腺癌细胞表面抗原的特殊细胞,再将其重新回输至患者体内,为T细胞识别和消灭前列腺癌细胞助一臂之力。

Provenge于2010年被FDA所批准,但由于Dendreon错误的销售战略和竞争对手的接连上市,2013年的业绩惨淡,最终被Valeant公司买下所有权。
虽然Provenge出师不利,但它的出现提示了人们癌症疫苗的未来的可能性。不少公司纷纷效仿,投入到癌症疫苗的开发中。
目前主要有美国Northwest Biotherapeutics研发的脑癌疫苗,处于临床3期;依阿华州的Newlink Genetics研发的用于治疗胰腺癌、非小细胞肺癌和黑色素瘤的疫苗,多处于临床二期或三期;inovio公司的宫颈癌疫苗、前列腺疫苗和乳腺癌疫苗;Aduro Biotech公司采用细菌而非病毒作为疫苗载体,主要用于胰腺癌、间皮瘤、胶质瘤、肺癌剂前列腺癌等。
除常规疫苗外,还有另辟蹊径的溶瘤病毒疫苗,将溶瘤病毒经基因改造后特异性感染肿瘤细胞。目前全球范围内上市的溶瘤病毒疗法中,除了2006年通过CFDA审批并获得生产资格的中国上海三维生物的H101一项之外,Amgen的Imlygic也在2015年10月获批上市。
截至到2013年底,全球范围内在研的癌症疫苗共有470个,靶标涵盖了从癌基因、癌蛋白到癌症发展过程中上皮间质转化(epithelial-mesenchymaltransition)和血管生成等事件的相关分子。免疫疗法的联合治疗将是未来肿瘤治疗的主导方向,扮演着“教官”角色的癌症疫苗无疑在这方面具有光明的前景。
3. 免疫检查点抑制剂
2015年4月,一篇刊登在医学权威杂志《NEJM》上的文章引起巨大的轰动。一名49岁的女性溃烂性黑色素瘤患者,在过去4年间两次手术切除肿瘤后均发生了转移复发,最终在左乳下产生了一处巨大的转移瘤。但在接受CTLA4抑制剂Ipilimumab与PD-1抑制剂Nivolumab联合注射的三周后,这个反复转移的巨大肿瘤就迅速消退了,消失速度之快令人瞠目结舌,甚至连伤口都来不及愈合。给药六周后的CT检查显示,胸壁上巨大的肿瘤已经完全不见了踪影。
作为癌症免疫治疗家族最年轻的成员,免疫检查点抑制剂(Immune checkpoint inhibitors, ICIs)自诞生起便为我们带来了源源不断的惊喜。
1987年,法国科学家发现了一类表达于T细胞表面的蛋白CTLA4,接种了肿瘤细胞的小鼠注射CTLA4抗体后,小鼠体内的肿瘤完全消退。免疫检查点抑制剂的雏形由此诞生。
1992年,日本京都大学本庶佑教授发现了PD-1,1999年美国耶鲁大学教授Lieping Chen发现了PD-L1,与 CTLA4一起构成了免疫检查点蛋白家族。这些免疫检查点被激活时能抑制T细胞的增殖和功能,使肿瘤细胞逃避免疫系统的检测和攻击。免疫检查点抑制剂的出现,有效阻断了通路,可有力的杀伤肿瘤细胞。
2009年, Bristol-Myers Squibb(BMS)收购了美国生物公司Medarex,连同它研发的PD-1抑制剂。这笔交易也被认为是癌症免疫疗法历史上最重要的一起收购。2014年7月,BMS的PD-1抑制剂Nivolumab在日本获批上市,被用于黑色素瘤的治疗。同年9月,FDA批准Merck的PD-1抑制剂pembrolizumab上市。
目前FDA已批准5款PD-1/PD-L1产品上市:
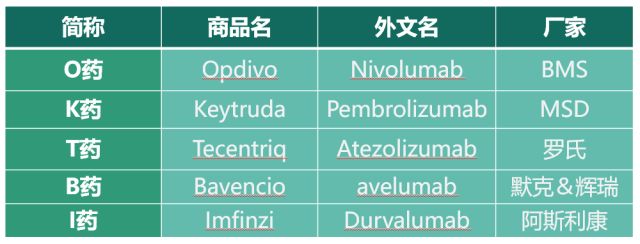
根据Decision Resources的预测,ICIs市场将在2020年达到70亿美元的规模,其中PD-1抑制剂将占据最大的份额。而随着人们对于免疫检查点认识的不断深入,以IDO1、KIR、LAG3等为靶点的新型ICIs逐渐走向了临床,也吸引了包括Pfizer、Merck KGaA等其他跨国药企的纷纷入场。可以想见在这样一个群星云集的细分市场里,最终的竞争结果在很大程度上将改变医药市场的格局,让我们一同拭目以待。
4. 过继性细胞疗法
1984年,身患晚期转移性恶性黑色素瘤的Linda Taylor在绝望之际第一次接受了癌症免疫学家Steven Rosenberg的治疗,将其淋巴细胞经大剂量的IL-2刺激,形成淋巴因子活化杀伤细胞(lymphokine-activated killercell,LAK cell),并重新会输至Taylor体内。然而令人意想不到的是: Taylor被LAK疗法完全治愈了!30多年后,Taylor依旧健康,回过头去,想必她一定会为当初的选择疯狂打CALL。
而在这30年来,过继疗法也从第一代的LAK疗法,经细胞因子活化杀伤细胞CIK疗法、肿瘤浸润淋巴细胞TIL疗法、细胞毒性T淋巴细胞CTL疗法到第五代嵌合抗原受体T细胞CAR-T和肿瘤特异性T细胞受体基因工程细胞TCR-T的技术变革。
下一篇:不敢相信,医生竟是自杀率最高的职业! 上一篇:外科医生一动笔,虐哭一批画画的